„Wir haben es einfach versucht und es hat geklappt“, waren die bescheidenen Worte mit denen Yamanaka die bahnbrechenden Experimente seiner Arbeitsgruppe im Jahr 2006 kürzlich gegenüber dem Deutschlandfunk, dem nationalen Hörfunkprogramm des Deutschlandradios, beschreibt. Dem Team gelang es damals am reproduktionsmedizinischen Institut der Universität Kyōto, iPS-Zellen (induzierte pluripotente Stammzellen, Anm.) aus Bindegewebszellen von Mäusen zu erzeugen.
Ein Jahr später gelang der Arbeitsgruppe dasselbe Experiment auch mit menschlichen Bindegewebszellen. Grundlage dafür war die Erkenntnis Yamanakas, dass der Zustand jeder Zelle darüber reguliert ist welche Eiweiße sie exponiert. Werden diese Eiweiße reguliert und durch Viruspartikel, die mit vier Genen beladen sind (Oct4, Sox2, c-Myc und Klf4) infiziert, können sich diese Zellen wieder in einen Zustand zurückentwickeln, in dem sie kurz nach der Befruchtung waren. Sie können sich dann weiter zu Neuronen, Muskeln oder Blutzellen verwandeln. Das alles ist in der Zellkulturschale möglich.
Weg für Organoid-Forschung geebnet
Der Umstand, dass Embryonen für die Stammzellenforschung zerstört werden mussten, war ein großer Motivator für Yamanakas Forschung, wie er sagt und weist auf die medizinischen und ethischen Hürden hin, die damit einhergingen. „Deshalb wollten wir Stammzellen erzeugen, die nicht aus menschlichen Embryonen stammen, sondern aus eigenen Körperzellen von Patient:innen“, so Yamanaka gegenüber Deutschlandfunk.
Die Methode des Japaners ist ethisch weniger umstritten und hat den Vorteil, dass sich die Zellen rasch von jeder Person aus der Haut oder dem Blut herstellen lassen. Zudem werden sie vom jeweiligen Immunsystem als eigene Zellen erkannt, da sie vom eigenen Körper und nicht von einem fremden Embryo stammen.
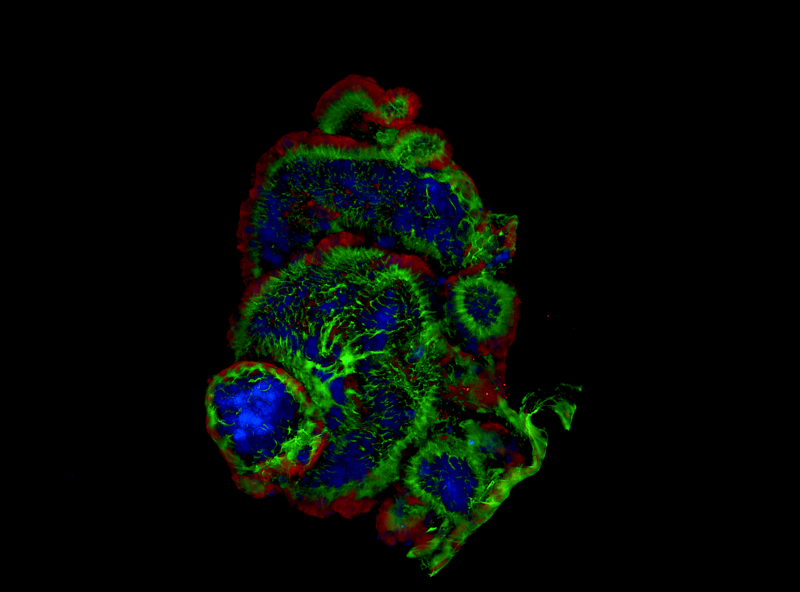
Damit eröffnete der Japaner auch einen neuen Weg zur Erforschung des menschlichen Gehirns. Auf seiner Methode aufbauend konnten etwa Forscher des Instituts für Molekulare Biotechnologie (IMBA) in Wien Stammzellen zu künstlich hergestellte Gehirn-Organoide im Labor wachsen lassen. Organoide ermöglichen medizinische Tests, für die bisher Tierversuche herangezogen wurden.
Krankheiten aus IPS-Zellen simulieren
Um ein Organoid zu züchten, erzeugen Forscher mit dem sogenannten Yamanaka-Faktor aus pluripotenten iPS-Zellen ein Neuroektoderm (das Neuroektoderm ist der Teil des äußeren Keimblatts/Ektoderm, aus dem sich in der Embryonalentwicklung das Nervensystem entwickelt, Anm.). Die Stammzellen wachsen in einer Gewebskulturschale, werden entnommen und verklumpen sich zu einem Zellhaufen, den man auch Embryoid bodies nennt.
Dann kommen die Organoide in eine Substanz namens Matrigel (eine komplexe Mischung von Biomolekülen, die in der 3D-Zellkultur als Wachstumsgrundlage – Matrix, Zellsubstrat – verwendet wird, Anm.), in der sie sich entwickeln. Dort kommen die Organoide in ein Stadium, in dem sie histologisch wie ein menschliches Gehirn aussehen, anatomisch allerdings nicht.
Krankheiten simulieren
Die Forscher am IMBA waren eigene Angaben zufolge die Ersten, die gezeigt haben, dass man mit dreidimensionalen Kulturen aus iPS-Zellen Krankheiten simulieren kann. Am IMBA forschen mittlerweile fünf Gruppen an Organoiden. Ein Labor arbeitet mit Gehirn-Organoiden, Josef Penningers Labor mit Blutgefäß-Organoiden, eine Gruppe stellt Herz-Organoide her, eine andere Gruppe erstellt sogenannte Blastoide, welche die allerersten Schritte der menschlichen Entwicklung widerspiegeln und eine Gruppe erzeugt Darm- und Magen-Organoide.
„Auch wenn iPS-Zellen den embryonalen Stammzellen sehr ähnlich sind, zu 100 Prozent ident sind sie nicht“, wie Jürgen Knoblich, der als Molekularbiologe im IMBA forscht, ausführt. Aus diesem Grund werden nach wie vor beide Arten für klinische Studien eingesetzt – die ethische Diskussion ist also nicht vom Tisch.
Fokus auf Grundlagenforschung
Shin’ya Yamanakas Laufbahn begann mit dem Studium der Medizin, nach dessen Abschluss er als Assistenzart in der orthopädischen Chirurgie am Staatlichen Krankenhaus Ōsaka arbeitete. Zeitgleich war er Postdoktorand am Gladstone Institute of Cardiovascular Disease in San Francisco.
Seit der Gründung des Center for iPS Cell Research (CiRA) an der Universität Kyōto im Jahr 2010 war Yamanaka zwölf Jahre lang in sechs Amtszeiten als Direktor tätig. Ende März gab er bekannt, als Direktor des CiRA zurückzutreten. Er wolle mehr Zeit mit der Erforschung der iPS-Zellen verbringen, erklärte er den Rücktritt gegenüber der japanischen Zeitung „The Asahi Shimbun“. Er wolle sich mehr als bisher der Grundlagenforschung widmen, führte er aus.
Der Japaner will weiter seine Forschung als Professor am Institute for Integrated Cell-Material Sciences fortsetzen. Auch werde er die praktische Anwendung von iPS-Zellen weiter unterstützen, wie er bei einer Pressekonferenz im Frühjahr ankündigte. Zudem zeigte er sich überzeugt, dass Unternehmen in Zukunft eine wichtige Rolle bei der Anwendung von iPS-Zellen in der Praxis spielen werden.
Wegweisende Biotechnologien
iPS-Zellen und Organoide stellen eine Revolution in der Biomedizin dar. Andere Biotechnologien, die ebenfalls bahnbrechend waren, sind die Sequenzierung des menschlichen Genoms, wodurch sich Mutationen in Genen feststellen lassen und die Entwicklung der sogenannten Genschere CRISPR/Cas9, die es erlaubt bestimmte Mutationen in das Genom einzufügen oder diese zu reparieren.

IMBAMadeline%20Lancaster%EF%B9%96itok=Q88r1sg2.jpg)